Um átomo no estado fundamental possui todos os seus elétrons num estado de mínima energia (mais estabilidade). Quando o átomo estiver em sua forma neutra, ele tem número de elétrons igual ao número de prótons (o que facilita na identificação do elemento, sabendo simplesmente sua distribuição, já que cada átomo tem seu número atômico).
A distribuição dos elétrons no átomo deve ser feita na ordem de energia (indicada pelo sentido da seta no diagrama), do menos energético para o mais energético,
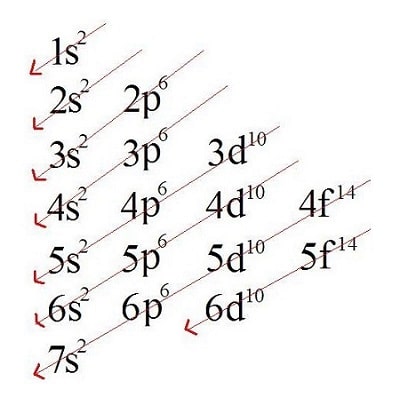 |
| Diagrama de Linus Pauling |
