Um átomo no estado fundamental possui todos os seus elétrons num estado de mínima energia (mais estabilidade). Quando o átomo estiver em sua forma neutra, ele tem número de elétrons igual ao número de prótons (o que facilita na identificação do elemento, sabendo simplesmente sua distribuição, já que cada átomo tem seu número atômico).
A distribuição dos elétrons no átomo deve ser feita na ordem de energia (indicada pelo sentido da seta no diagrama), do menos energético para o mais energético,
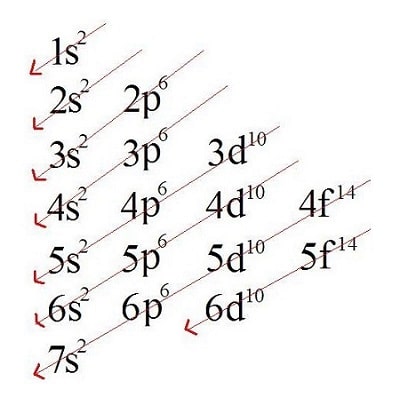 |
| Diagrama de Linus Pauling |
O diagrama escrito de forma contínua, isto é, de forma linear fica da seguinte maneira:
É importante citar que cada elemento da distribuição é composto de quatro números quânticos, principal (n), secundário ou azimutal (l), magnético (m ou ml) e spin (s ou mS).
Vale ressaltar que os elétrons estão submetidos ao principio da exclusão de pauli, isto é, não podem existir dois elétrons com os mesmos números quânticos.
- O número quântico principal (n) representa a camada em que o elétron está (por isso vai de um a sete). ["é o número da frente"]
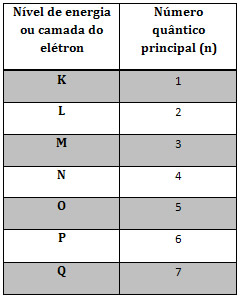
- O número quântico secundário ou azimutal (l) indica o subnível em que o elétrons está. ["É a letra"]
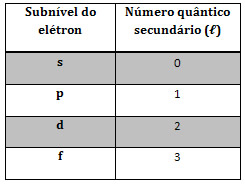
- O número quântico terciário ou magnético (m) Descreve a orientação do orbital no espaço. O número m pode ter qualquer valor inteiro entre +l e –l, inclusive zero.
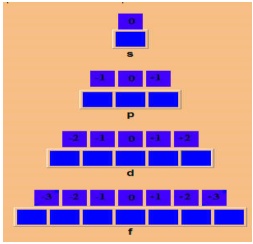
Para preencher o diagrama acima devemos usar a regra de Hund, isto é, Ao preencher os orbitais (caixinhas) de um mesmo subnível, os elétrons entrarão em orbitais vazios, até que cada orbital (caixinha) contenha um elétron. Somente então cada orbital (caixinha) receberá o novo elétron.
- O número quântico spin (ms) descreve o sentido de rotação do elétron (horária ou anti-horária) em torno de seu próprio eixo. O número ms pode ter somente os valores +1/2 e -1/2.
Distribuição nos íons
Fazer a distribuição para o átomo neutro e em seguida adicionar ou retirar elétrons.
Desse modo, a distribuição eletrônica do cátion Fe2+ é dada por: 1s2 2s2 2p6 3s2 3p6 3d6
obs: o "índice" representa o número de elétrons
obs2: o diagrama de linus pauling não acaba, ele é comumente terminado no 6d10 por conta de que não existe, ainda, um átomo com mais elétrons que 118
A fim de exercitar, faça a distribuição eletrônica dos seguintes átomo e indique seus quatro números quânticos.

Nenhum comentário:
Postar um comentário